阳明交通大学蔡明翰副教授团队最新研究显示,不论是擅长躲入B细胞且有致癌风险的EB病毒(EBV),还是喜欢潜伏在感觉神经且会造成口唇出现水泡并且反覆发作的第一型人类单纯疱疹病毒(HSV-1),GMI都能大幅降低病毒的感染率,其主要的作用机制是让病毒开启细胞大门的钥匙gB蛋白失灵,使得病毒就算已经黏附在细胞上,依然开不了细胞大门而难以登堂入室。
文/吴亭瑶

先前被证实能够抑制新冠病毒入侵细胞的小孢子灵芝免疫调节蛋白质GMI(Ganoderma microsporum immunomodulatory protein),如今又被证明可以对抗疱疹病毒。根据阳明交通大学微生物及免疫学研究所蔡明翰副教授团队2025年5月发表在《International Journal of Biological Macromolecules》(国际生物大分子杂志)的研究显示,GMI可以阻止两种类型的疱疹病毒遂行感染——其一是擅长躲入B细胞且有致癌风险的EB病毒(EBV),其二是喜欢潜伏在感觉神经且会造成口唇出现水泡并且反覆发作的第一型人类单纯疱疹病毒(HSV-1)。
该研究由蔡明翰副教授领军的肿瘤癌症病毒及病毒生物科技实验室〔包括本论文第一作者Di Ngoc Kha Vo(武玉可怡)第二作者Ho, Phan Thanh Ha(胡潘清霞)等五名研究生〕,联手阳明交通大学传统医药研究所林东毅教授、马来亚大学理学院生物科学研究所Yat-Yuen Lim副教授,以及卫福部国家中医药研究所资讯中心主任暨台北医学大学医学检验暨生物技术学系所蔡耿彰副教授等共同完成。
源自小孢子灵芝(Ganoderma microsporum)的GMI是由111个胺基酸组成、结构稳定、耐热耐酸、可被单独规格化量产的纯蛋白质,其在蛋白质资料库Protein Data Bank(PDB ID: 3KCW)和美国卫生研究院的化学分子与生物活性资料库PubChem(SID: 461501955)均登记有案。
2020年被美国FDA列为无保留意见的新膳食成分(NDI1133),2022年再被台湾卫福部核准为可供食品使用原料,说明GMI具备高度的食用安全性;其在发现之初就确认的双向免疫调节作用,以及十多年来被众多研究团队再三确认的体内抗肿瘤作用(尤其是抗肺癌),还有COVID-19疫情期间被意外发现可以经鼻吸入预防新冠病毒感染和相关肺炎,突显出GMI多方面的健康功效与实用价值。
【Part 1】GMI vs. EB病毒
GMI既可阻断EB病毒入侵上皮细胞
也能干扰EB病毒透过B细胞传播
以亲密接触(如亲吻)作为主要传播途径的EB病毒,通常都从口腔与咽喉的上皮细胞入侵体内,然後再躲进B细胞长期潜伏,待免疫低下时再重新活化,由被感染的B细胞将病毒传给不同部位(如鼻咽、胃部)的上皮细胞,干扰细胞的正常运作,进而引发细胞癌变。换句话说,如果能增强上皮细胞的防御能力,就有降低相关的致癌机会。(注:上皮细胞是构成皮肤和内脏最外层,以及口腔、呼吸道、消化道等各种腔道表层,还有血管内壁表层的细胞。)
本研究即观察到,GMI不论是跟EB病毒和上皮细胞一起培养(图1),还是跟带有EB病毒的B细胞和上皮细胞一起培养(图2),都能降低病毒入侵上皮细胞的机会,而且效果与GMI浓度呈正相关,显示GMI有保护上皮细胞防御EB病毒的作用。
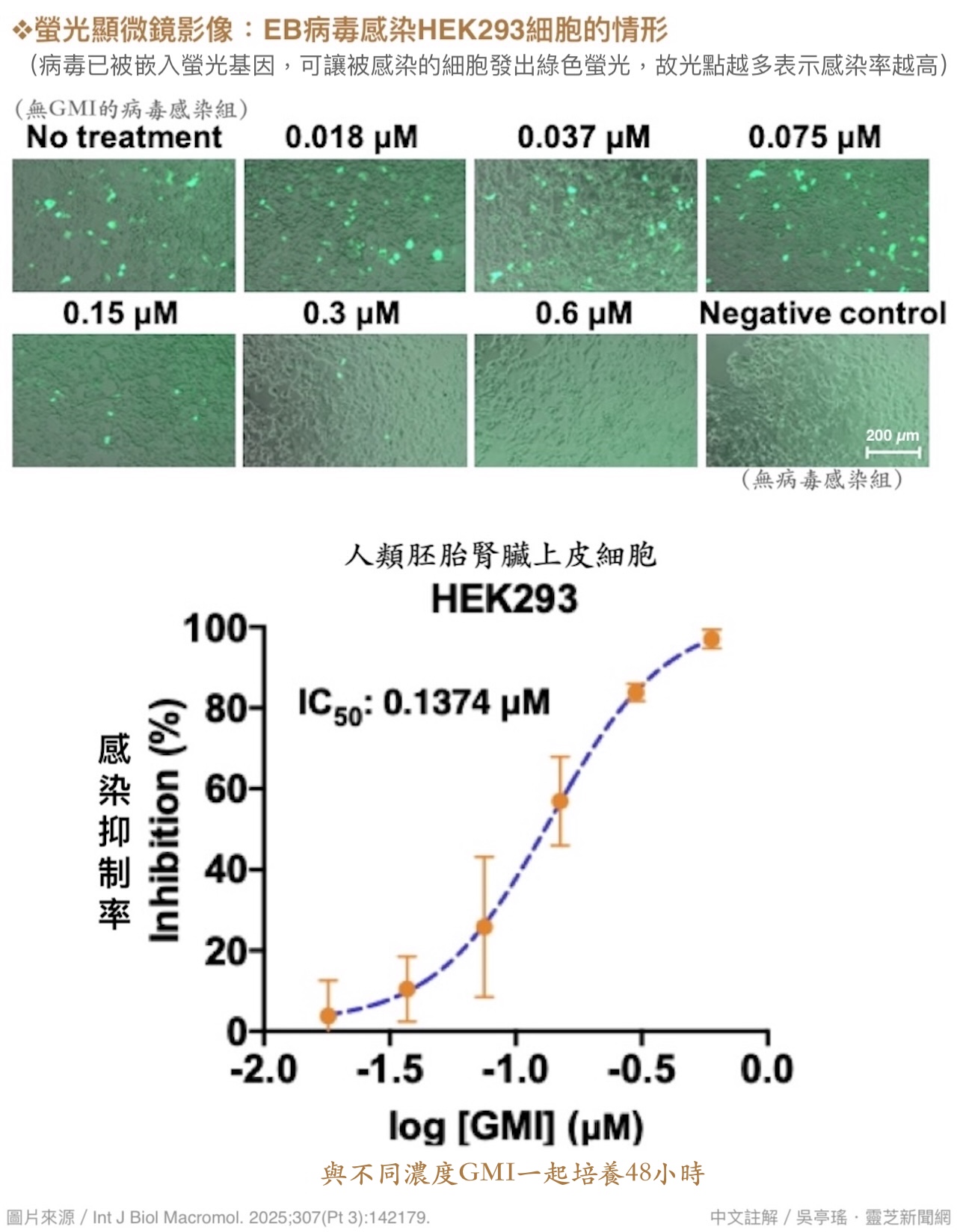
【图1】GMI可降低EB病毒对上皮细胞的感染率
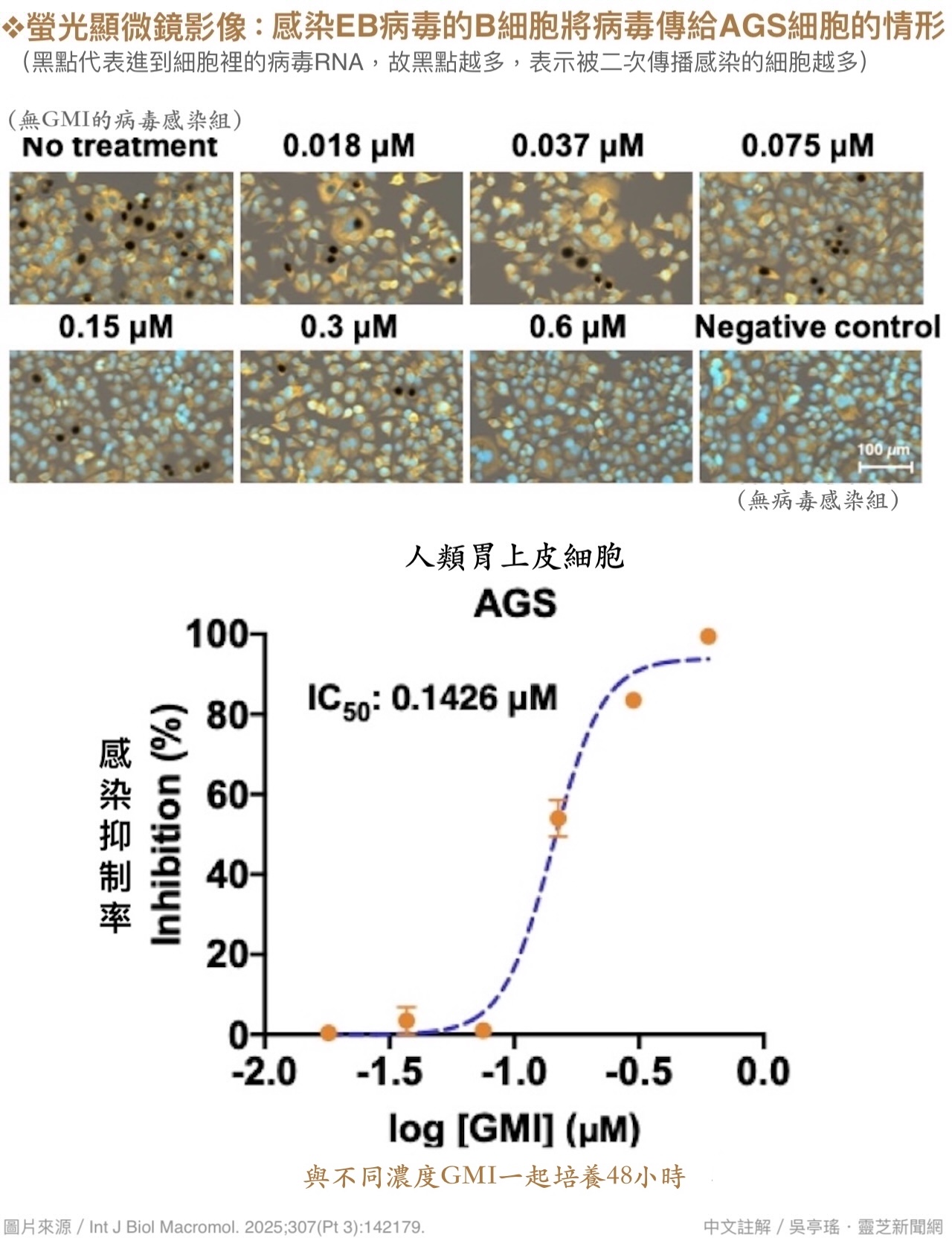
【图2】GMI可阻止EB病毒透过B细胞传给上皮细胞
GMI可抑制不同致癌特性的EB病毒
上述实验使用的EB病毒是偏好感染上皮细胞的「M81野生型(原生型)病毒株」,来自一名鼻咽癌患者。为了确认GMI抑制EB病毒的有效性是否会因不同毒株而有所差异,研究者另外还选用两种不同特性的EB病毒株,分别跟上皮细胞进行PK:其一是同样偏好感染上皮细胞,但与胃癌相关的YCCEL1病毒株;其二为偏好感染B细胞,与淋巴瘤相关毒株近似的MSHJ病毒株。
结果发现,这三种EB病毒在浓度0.6 µM的GMI介入下,几乎都无法造成细胞感染(图3),显示GMI抑制EB病毒感染可能具有某种程度的广效性。由於0.6 μM的GMI对实验所用的两种上皮细胞存活率并无显着影响(图4),亦即不会减少EB病毒入侵的潜在对象,因此GMI降低感染率的作用显然是透过其他方式达成的。
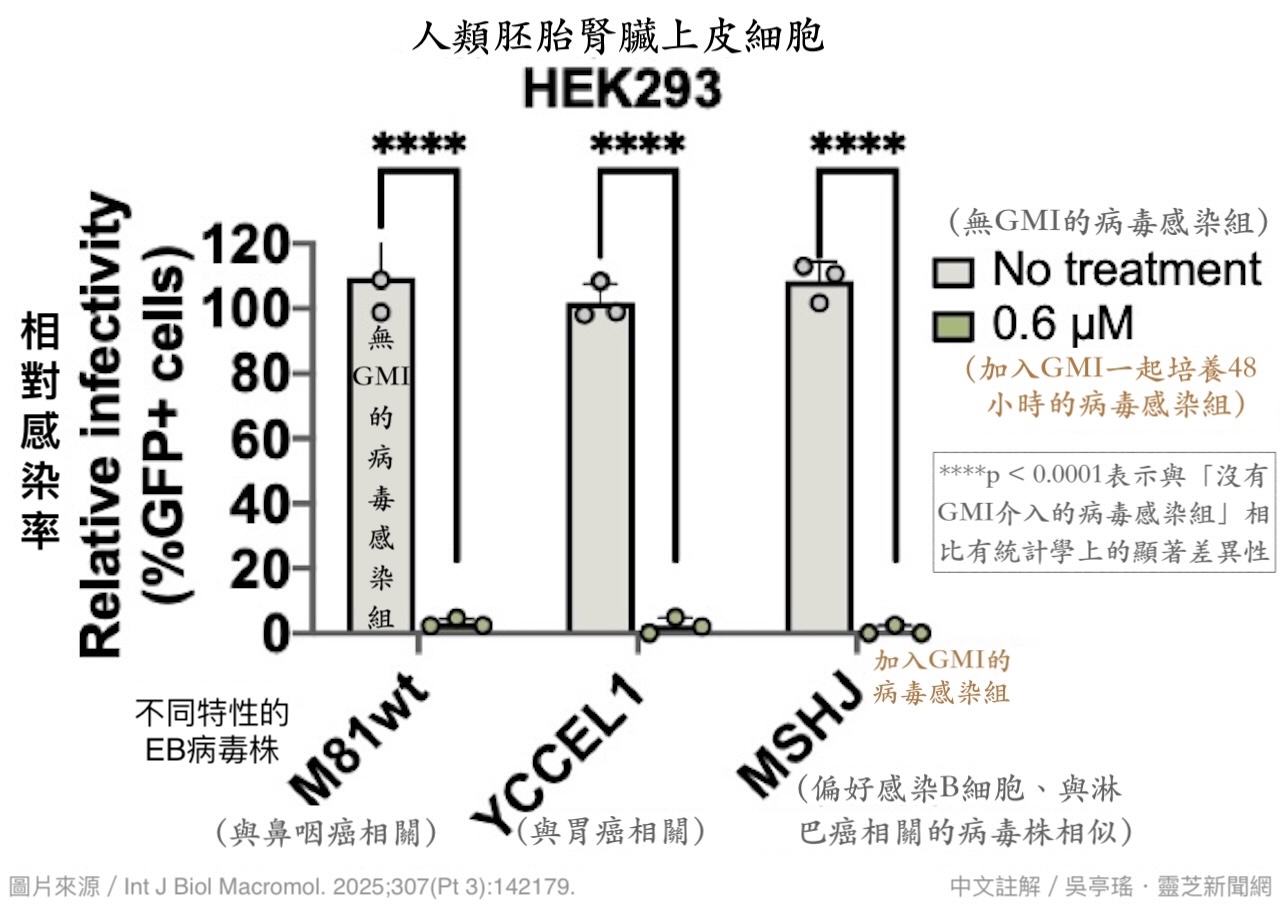
【图3】GMI对三种特性的EB病毒都有抗感染作用
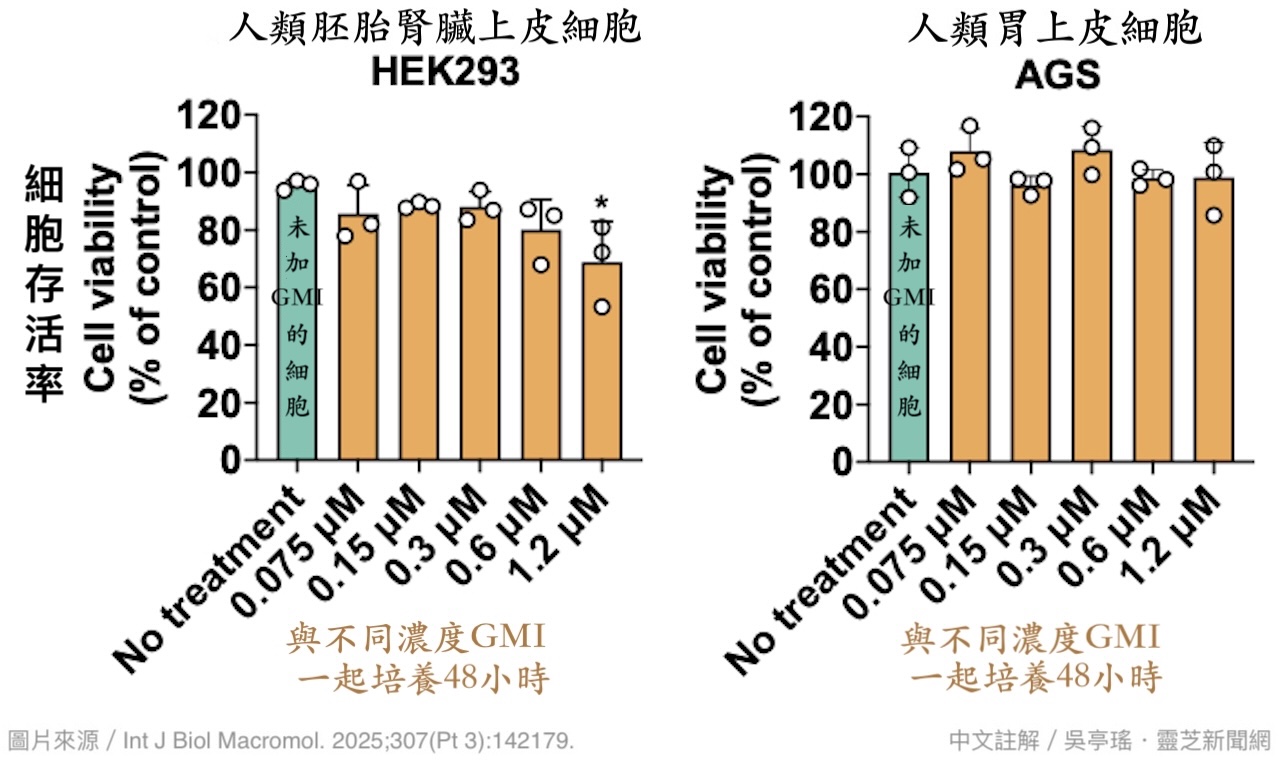
【图4】GMI抗EB病毒的有效浓度(0.6 µM)
对上皮细胞存活率并无显着影响
GMI可干扰EB病毒与细胞的膜融合
阻止已经兵临城下的病毒登堂入室
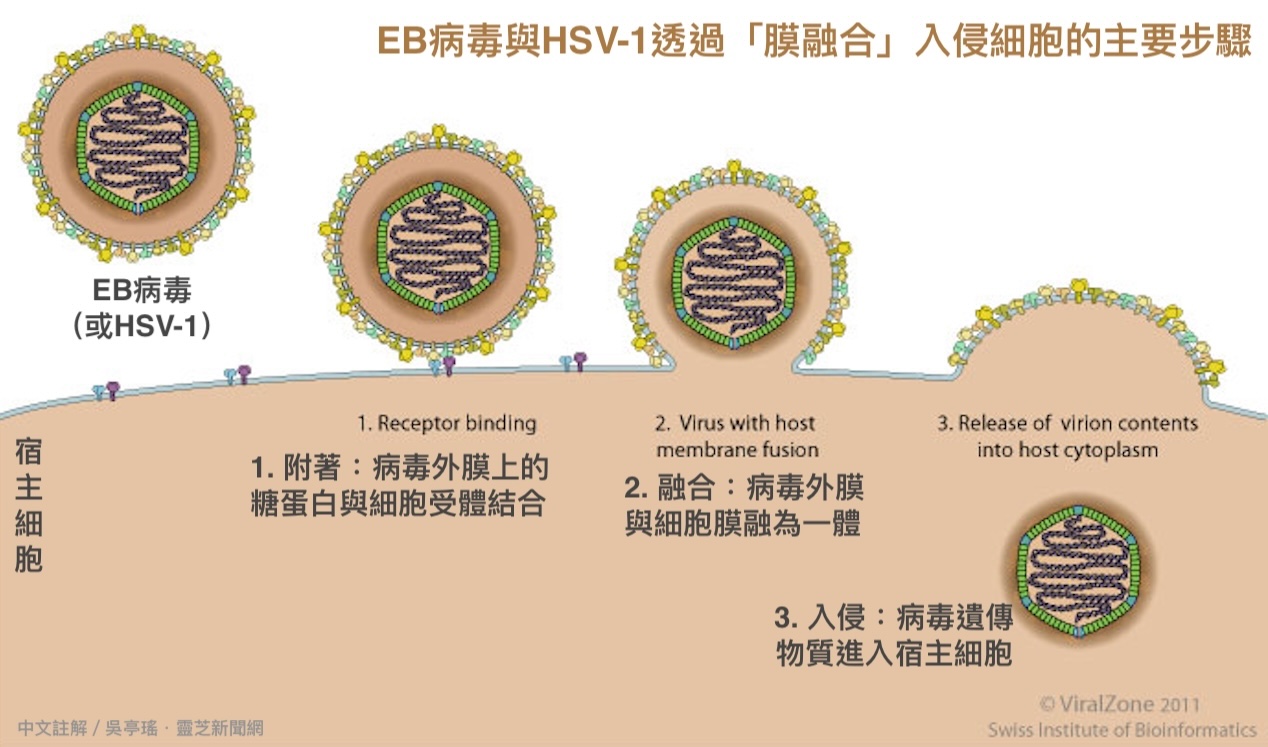
对EB病毒和後续实验会提到的HSV-1来说,它们对细胞的感染可以分成几个阶段:附着(病毒蛋白与细胞受体结合),膜融合(病毒外套膜与细胞膜融为一体),入侵(病毒的遗传物质进到细胞里),复制(劫持细胞复制新的病毒颗粒),以及二次传播(释出病毒生力军去感染更多细胞)。当病毒无法附着在细胞上,或不得其门而入,或复制过程受阻,或新生病毒被锁在细胞里,都影响病毒的感染效率。
所以GMI抑制EB病毒感染的作用主要发生在哪个阶段?根据本研究的实验显示,当EB病毒接触细胞之初(还没进入细胞之前)就有GMI存在,对感染的抑制效果最好(可减少近75%的细胞受到感染),远胜病毒已经入侵细胞才加入GMI亡羊补牢。不过GMI并未影响EB病毒附着细胞的能力,其抗感染作用主要来自「阻止EB病毒与细胞之间的膜融合(membrane fusion)」。
膜融合是EB病毒(还有第一型单纯疱疹病毒HSV-1)入侵上皮细胞的主要方式,过程中需要病毒外膜上的多种糖蛋白(glycoprotein)和细胞表面的受体相互协作。其中,病毒外膜上的gB(glycoprotein B,糖蛋白B)负责执行膜融合的动作,故有「融合蛋白」之称;而上皮细胞表面的EphA2受体则有促进膜融合的作用,可以大幅提高病毒进入细胞的效率。
根据本研究的实验发现,GMI不但能与gB结合,也能与EphA2结合,此作用会让干扰二者原本的活性与功能,进而让膜融合的过程无法进行或效率变慢,使得已经兵临城下的病毒无法顺利地打开细胞大门登堂入室(图5)。
(https://viralzone.expasy.org/987?outline=all_by_species)
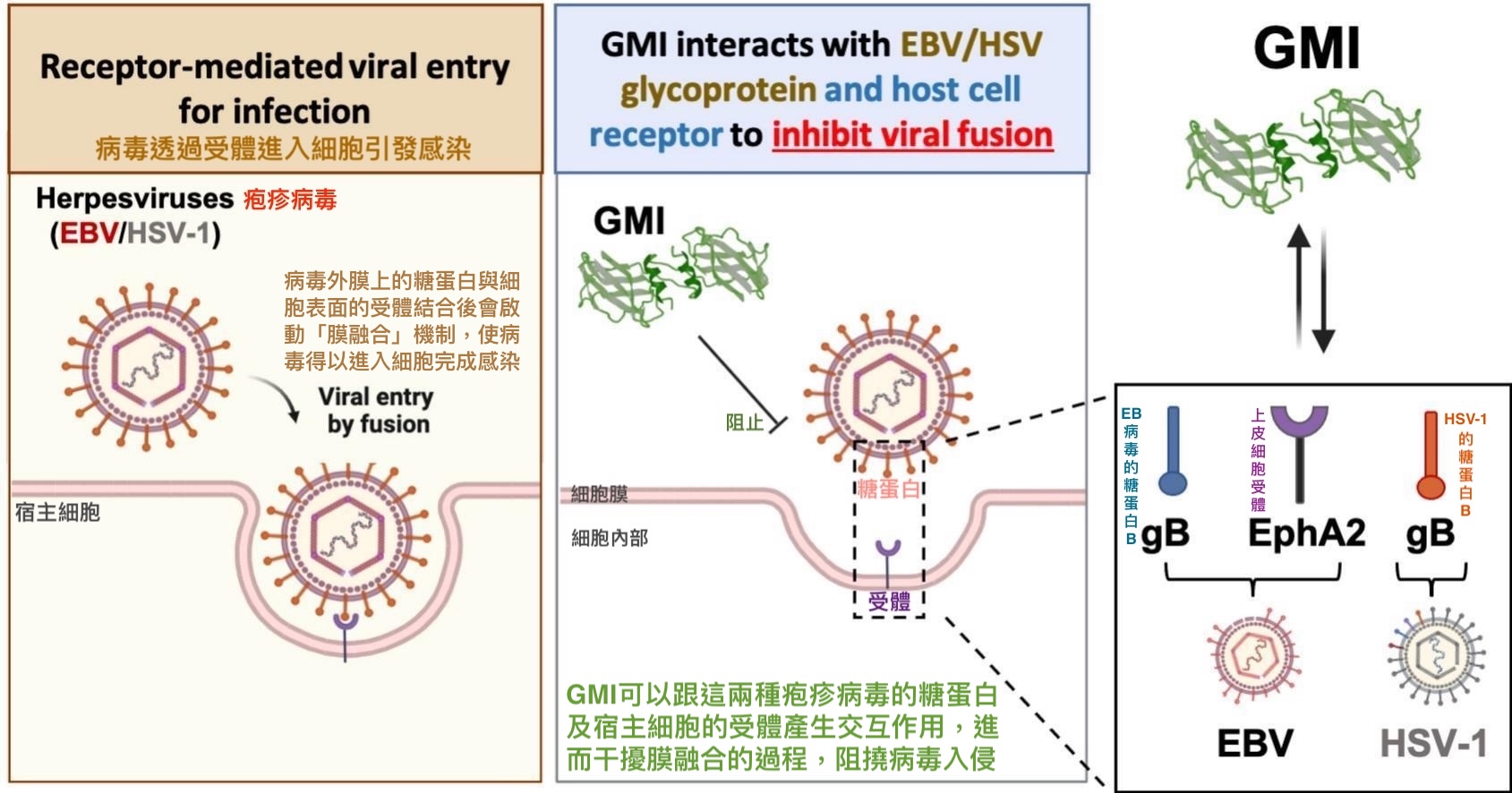
【图5】GMI阻止EB病毒和HSV-1入侵细胞的机制示意图
GMI也能阻挠EB病毒感染B细胞
如前所述,B细胞是除了上皮细胞之外,另一个被EB病毒锁定的攻击目标。尤有甚者,B细胞同时也是EB病毒进到体内之後躲避免疫系统追缉的藏身之所,长期被EB病毒挟持的B细胞除了可能在未来(免疫低下时)成为EB病毒再次活化後的复制工厂,更可能被EB病毒转化成永生不死的癌细胞。
本研究使用人类初代B细胞(直接从人体周边血分离而得的新鲜B细胞)测试GMI在EB病毒环伺下对它们的保护作用,结果几乎跟GMI保护上皮细胞的效果如出一辙(图6),而且抑制感染的主要作用阶段也是发生在EB病毒刚接触B细胞的前几小时。
由於实验还发现GMI并不能阻止EB病毒附着在B细胞上,因此研究团队合理推测,GMI阻挠EB病毒入侵B细胞的关键,应该也是跟「GMI结合EB病毒的gB蛋白,进而干扰病毒膜融合的过程」有关。
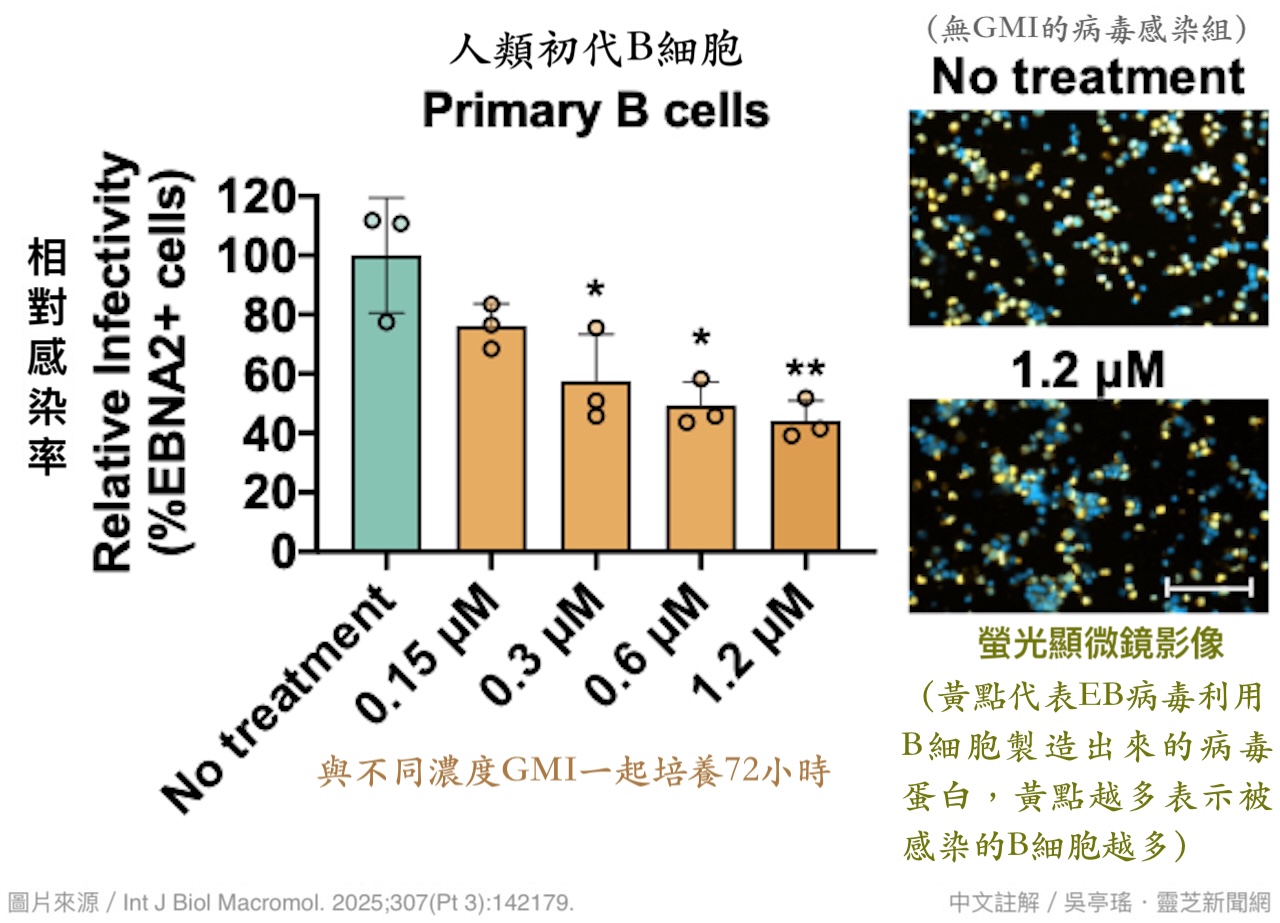
【图6】GMI可降低EB病毒对B细胞的感染率
【Part 2】GMI vs. 第一型人类单纯疱疹病毒HSV-1
GMI可阻止HSV-1感染上皮细胞
HSV-1跟EB病毒都能经由唾液传播的疱疹病毒,也都具有结构与功能相似的融合蛋白gB,所以研究团队也检测了GMI对抗HSV-1的能力。结果发现,GMI确实可以跟HSV-1的gB蛋白紧密结合,而且可以在浓度0.6 µM的条件下(就如GMI抑制EB病毒感染上皮细胞的有效剂量一样)阻止HSV-1感染上皮细胞,其效果甚至显着优於专门用来阻止HSV-1与细胞膜融合的中和抗体(图7)。
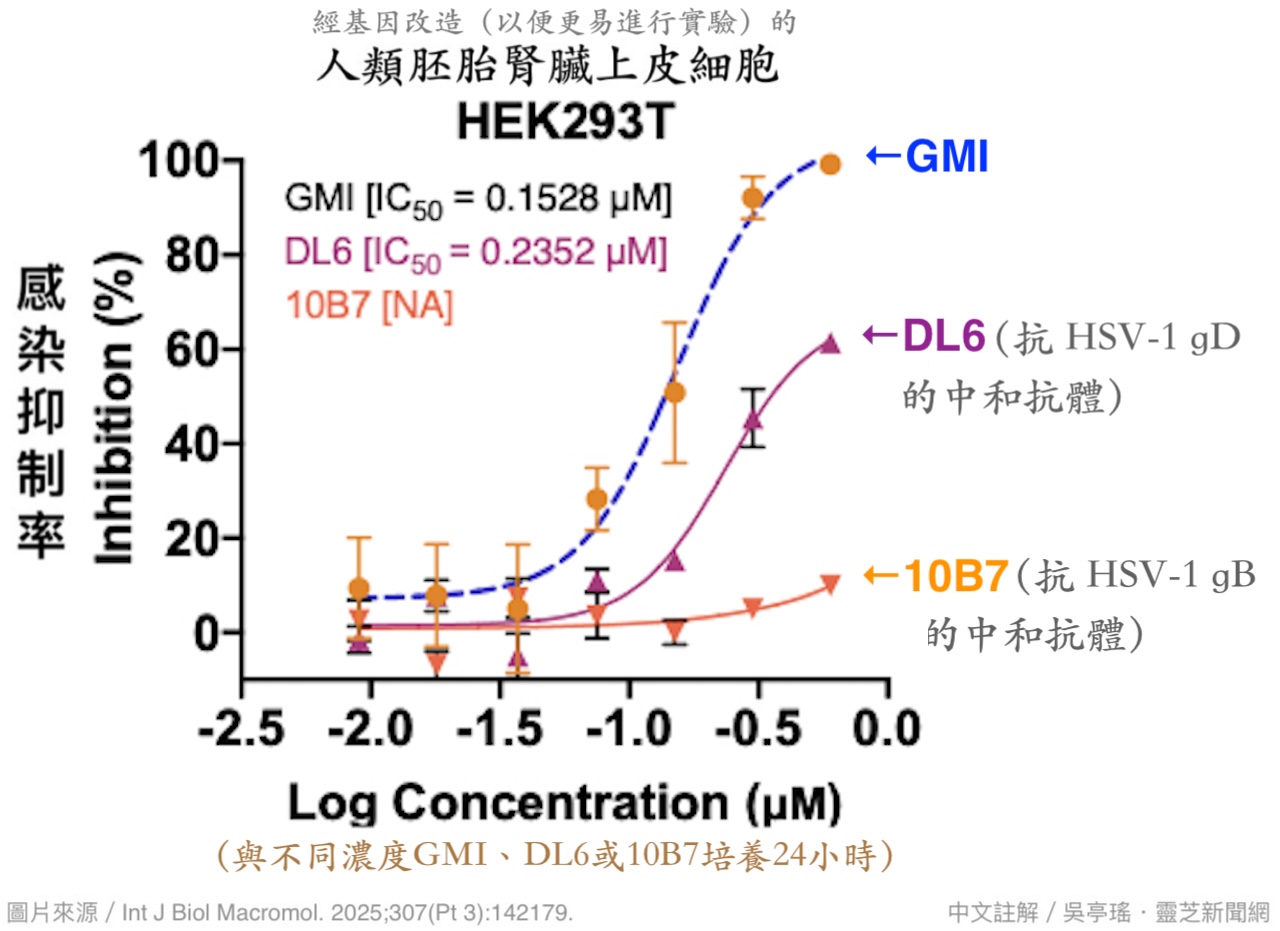
【图7】GMI抑制HSV-1感染上皮细胞的效果
优於研究用途的中和抗体DL-6和10B7
GMI抑制HSV-1感染的作用机制:
病毒不易附着细胞,也不易透过膜融合入侵细胞
上述实验所用的中和抗体DL6和10B7主要是让病毒侵犯细胞必要的两种糖蛋白失灵:前者针对负责与细胞表面受体结合进而引发後续融合反应的gD(糖蛋白D),後者针对实际执行膜融合的gB(糖蛋白B)。然而GMI不管在何种浓度下的抗感染效果都在它们之上(图7),显示GMI抑制HSV-1感染上皮细胞不仅是透过干扰病毒与细胞膜融合单一机制,而是还有其它作用机制参与。
果不其然!经研究团队进一步探究发现,相较於GMI抑制EB病毒感染细胞主要是发生在病毒进入细阶段,GMI对HSV-1附着细胞和进入细胞都有很显着的抑制作用——可使附着细胞表面的病毒量减少85%,也能使膜融合的发生率降低近70%(图8)。
因此,只要在病毒接触细胞早期加入GMI,都能大幅降低上皮细胞的感染率。实验还发现,先经GMI洗礼两小时再接触HSV-1的上皮细胞,即使在病毒挑战过程中没有GMI护航,也能提高细胞对病毒的防御力。但最好的抗感染效果则是在HSV-1尚未出现前就用GMI保护细胞,并且在HSV-1威胁期间仍持续使用GMI护航,那麽被感染的细胞将变得少之又少(图9)。
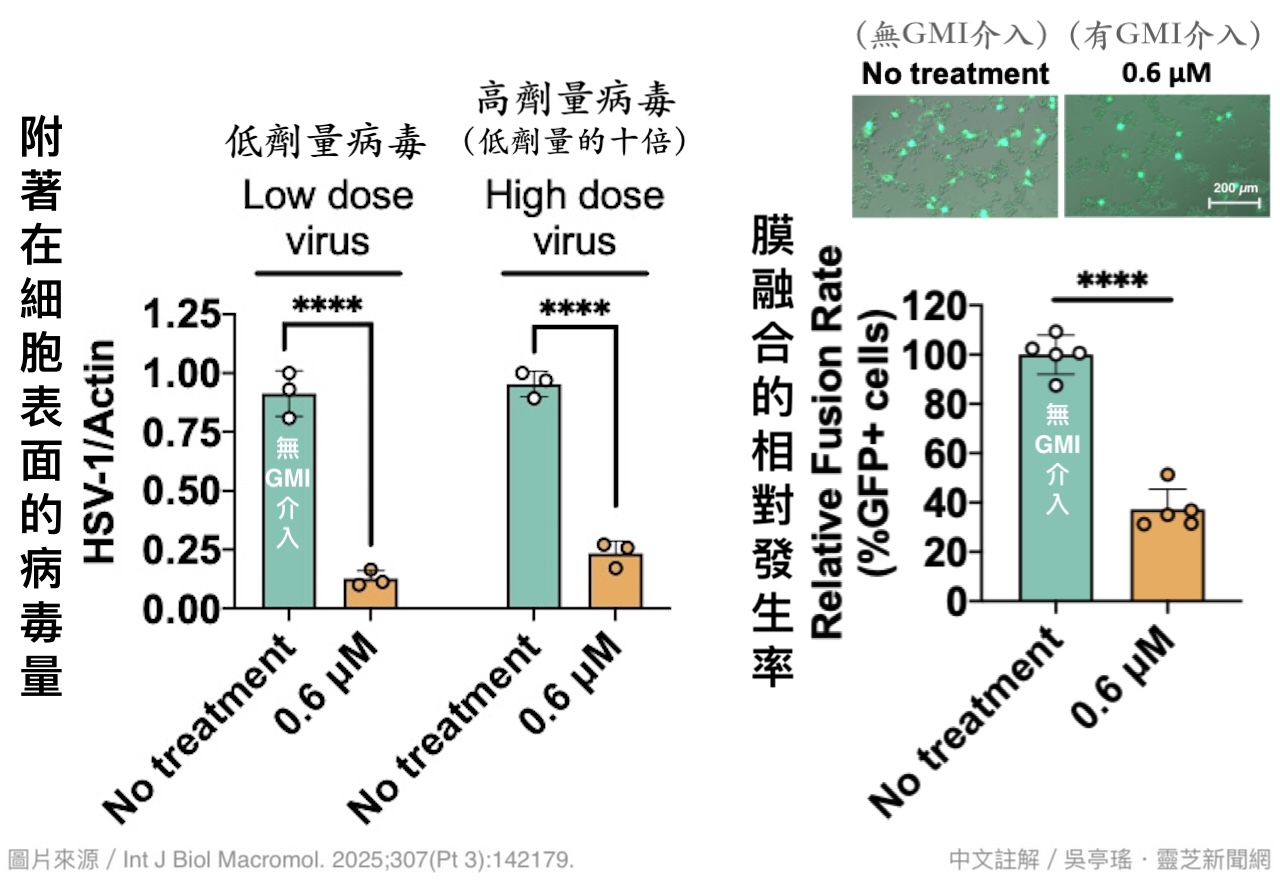
【图8】GMI对於HSV-1附着上皮细胞(左图)
与膜融合(右图)的抑制效果
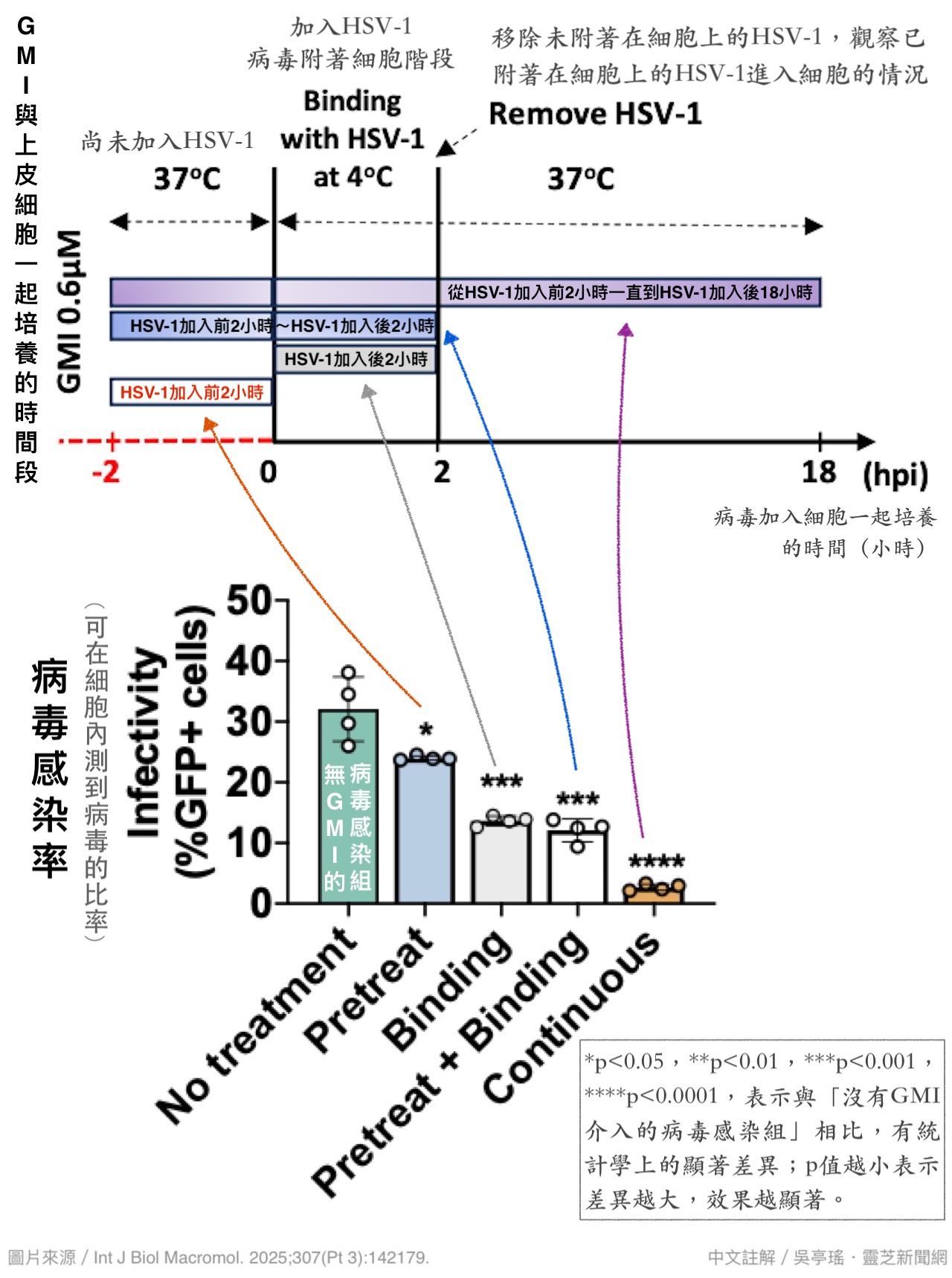
【图9】GMI在不同时间段介入对HSV-1感染上皮细胞的抑制效果
【Part 3】GMI抗疱疹病毒的独特之处
GMI结合融合蛋白gB的机制
赋予它抗疱疹病毒的广效性
gB蛋白的Domain I是病毒执行膜融合的活性核心区域,EB病毒与HSV-1主要就是依靠这个区域与细胞膜结合,进而将病毒的遗传物质送入细胞。当gB蛋白的这个区域结合了其它物质(如GMI),就会阻碍它跟细胞膜的结合——就像原本能够开门的钥匙,因为结构改变而无法插入或转动门锁。
本研究透过AI工具进行的结构预测分析即显示,GMI与gB蛋白的结合位点正好就集中在这个区域(图10),此一发现无疑为GMI抑制EB病毒与HSV-1感染的作用再添一项有力证据。
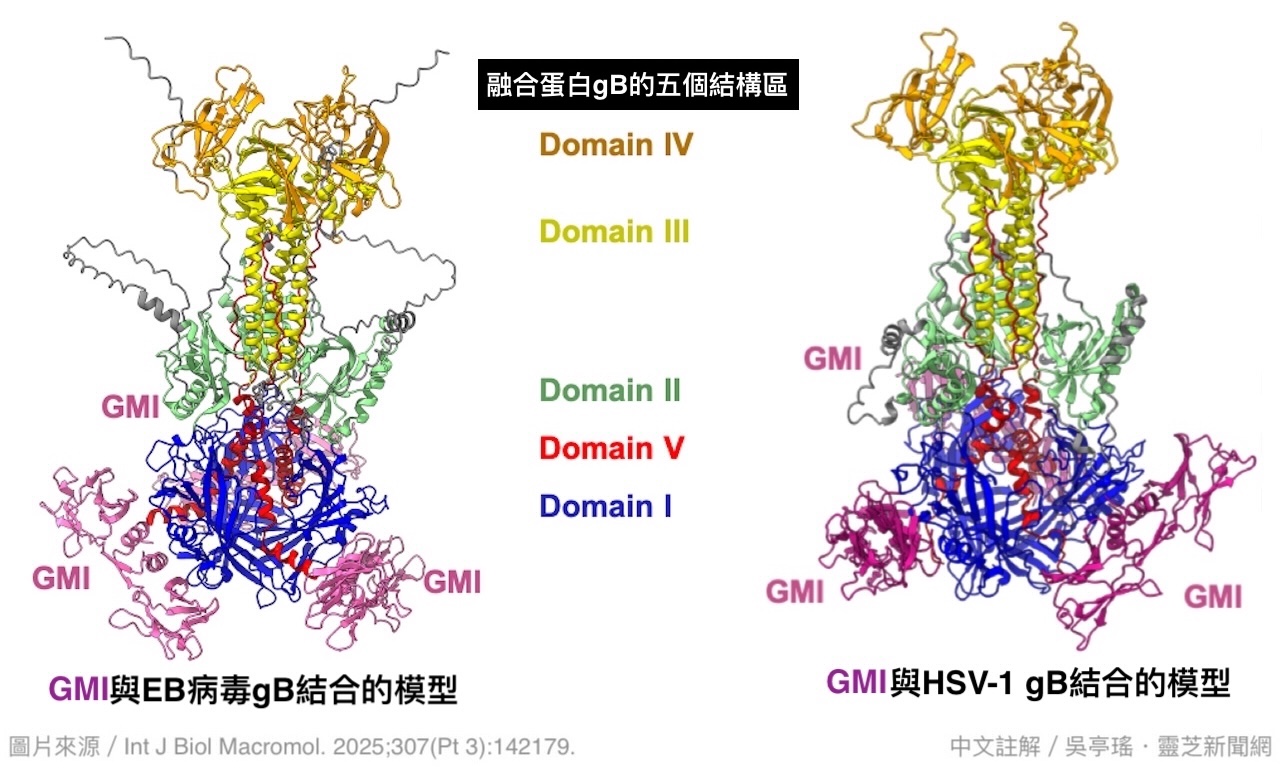
【图10】AI模拟GMI与疱疹病毒融合蛋白gB的结合位点
本研究还发现,另一种同样能经由唾液传播的疱疹病毒——巨细胞病毒(HCMV)——其负责执行膜融合的gB蛋白也能跟GMI结合。
疱疹病毒在生物分类学上有α、β、γ三种亚型,HSV-1、巨细胞病毒与EB病毒刚好分属这三种亚型,本研究又证明GMI都能跟它们的gB蛋白结合,加上gB蛋白在疱疹病毒家族中具有高度的结构保守性(亦即这种蛋白在不同疱疹病毒之间的关键结构几乎一样,且在演化过程中维持稳定、不易改变),因此研究团队推测,GMI抗感染的有效性可能不只局限在实验所用的几种疱疹病毒,而是会对整个疱疹病毒家族都有抑制潜力。
GMI预防感染的作用类似疫苗
不同於现有抗病毒药物
综合上述研究成果可知,GMI是少数能同时针对三大疱疹病毒亚型(α、β、γ)发挥抑制作用的单一蛋白质,其结合gB蛋白活性区进而导致病毒无法透过膜合进入细胞的机制,让GMI可以发挥「预防感染」的作用,其与现有抗病毒药物主要都是针对入侵细胞後的复制过程进行干扰或抑制的「感染後再设法防堵」全然不同,而这种「预防感染」的作用正是GMI抗病毒的独道之处。
回头看之前GMI被科学证明的抗新冠病毒(SARS-CoV-2)作用,是促使细胞把ACE2受体收到细胞内,让病毒不得其门而入;这回GMI被科学证明的抗疱疹病毒作用,则是让病毒开启细胞大门的钥匙gB蛋白失灵,使得病毒就算已经黏附在细胞上,依然开不了细胞大门而难以登堂入室。此二者的异曲同工之妙,无不暗示GMI有类似疫苗的保护效果。
GMI的食品原料和膳食成分的安全性,让GMI抗病毒的研究成果有机会落实在日常生活里,而不只是一时研究兴起的画饼充饥。如果再考虑GMI还同时具备抗癌广效性,以及对提升免疫力与抑制异常发炎的双向调节性,那麽形容GMI就像创造天选之人的天选之材,或许并不为过。
〔资料来源〕Di Ngoc Kha Vo, et al. Broad-spectrum antiviral activity of Ganoderma microsporum immunomodulatory protein: Targeting glycoprotein gB to inhibit EBV and HSV-1 infections via viral fusion blockage. Int J Biol Macromol. 2025 Mar 16;307(Pt 3):142179. doi: 10.1016/j.ijbiomac.2025.142179.


