乾癣虽然不会直接致命,但是一种终身性疾病,其症状会随压力、感染、季节变化等因素波动,即便治疗後症状有所缓解也可能突然复发,因此患者需要一种能长期稳定病情且相对安全的调理方式。源自灵芝(Ganoderma lucidum)菌丝体且可被规格化量产的免疫调节蛋白 LZ-8(Ling-Zhi 8)或许就有这方面的应用潜力。
文/吴亭瑶

俗称牛皮癣或银屑病的乾癣(psoriasis)是一种免疫系统异常引起的慢性发炎性皮肤病。目前已知其发作通常受遗传与环境因素影响,由於某些皮肤创伤、感染或药物的诱发,使T细胞调节紊乱,持续释放某些促发炎的细胞激素,刺激了位於表皮基底层的角质细胞,使其快速增生,并使未成熟的角质细胞迅速被推向皮肤表层,最终不只导致表皮增厚、皮肤不断有鳞屑脱落,也使受发炎反应影响的皮肤区域出现乾燥的红斑。
根据台湾大学医学院免疫学研究所博士後研究员林志萱和朱清良教授等今年(2025)3月发表在《Biomedicine & Pharmacotherapy》(生物医学与药物疗法)的研究显示,预先并持续口服LZ-8调理一段时间的小鼠,可以诱过肠道耐受性树突细胞的调节作用,提高小鼠对於IMQ(Imiquimod,咪喹莫特)诱发类似人类乾癣症状的耐受力,减轻相关的发炎反应与皮肤症状。
IMQ会刺激免疫促进发炎,当它涂抹在小鼠皮肤时,可快速诱发类似人类乾癣的症状,是学界探讨乾癣相关议题常用的动物模型。在本研究中,小鼠背部皮肤在连续涂抹6天的IMQ後会出现红斑、脱屑、增厚等症状,但如果小鼠从涂抹IMQ前7天就开始口服LZ-8(每天10 mg或20 mg),并在涂抹IMQ期间持续服用,则相关症状都比较轻,且效果与LZ-8用量呈正相关(图1A~C)。
乾癣的发病机制主要跟T细胞亚群中的Th1和Th17过度活化,以及负责抑制发炎的Treg(调节性T细胞)不够有力有关。上述动物实验即可观察到此现象:连续涂抹IMQ会造成小鼠脾脏里的 Th1、Th17细胞激增,Treg细胞略减,由它们分泌的细胞激素在血液与皮肤里也有相应的变化,但这些反映发炎加剧的指标在LZ-8保护的小鼠身上却没那麽严重(图1D~E)。
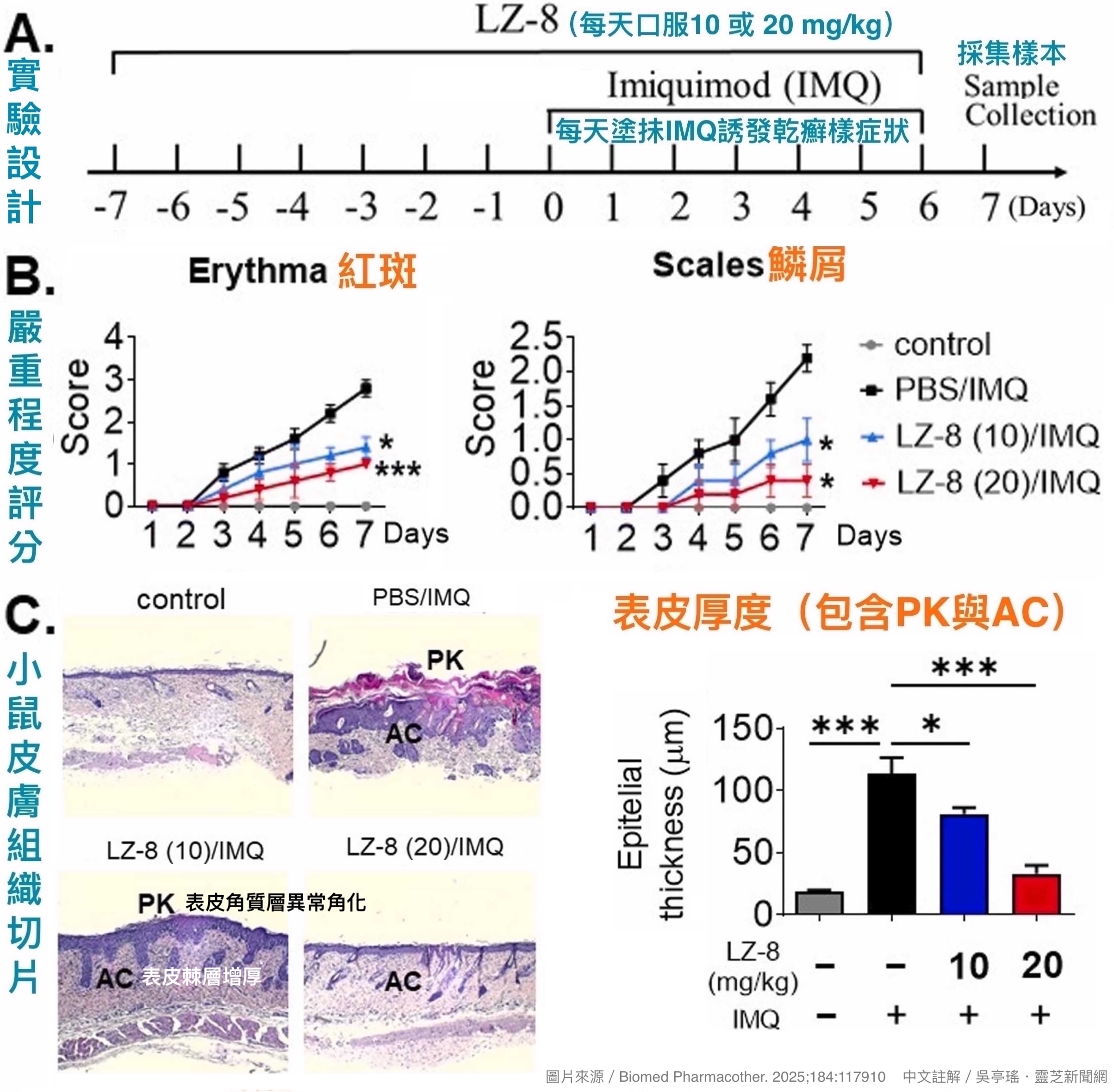
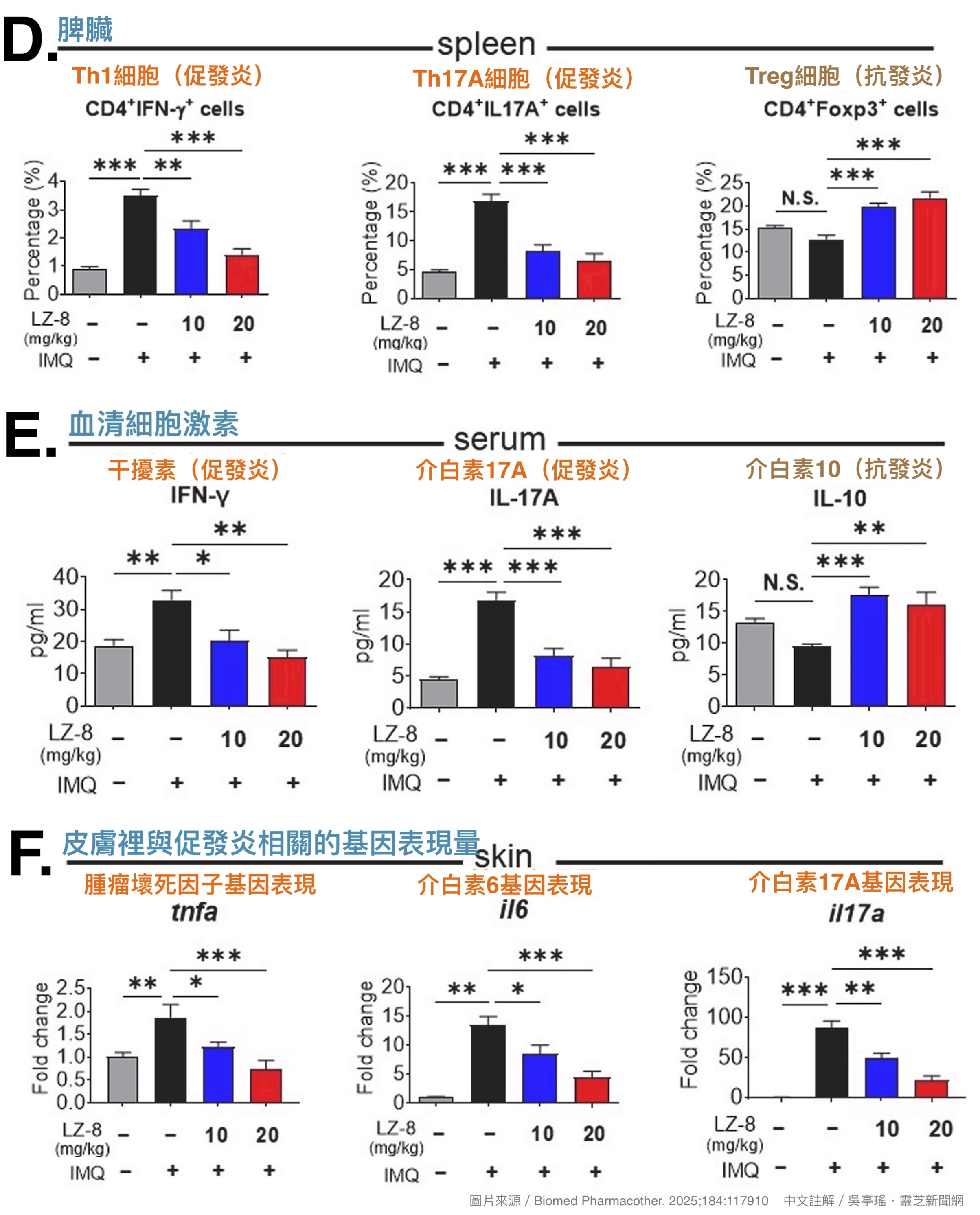
【图1】以IMQ诱发小鼠皮肤产生类似人类乾癣症状,预先口服并在诱发期间持续服用LZ-8的小鼠,皮肤出现红斑、脱屑和增厚的情况明显较轻;脾脏、血清与皮肤的促发炎相关指标比较不易增加,但抗发炎相关指标则相对较高。(*p<0.05, **p<0.01,***p<0.001,代表与「未用LZ-8但有以IMQ诱发症状」的PBS/IMQ组相比有显着差异)
本研究还进一步探讨了LZ-8调节T细胞的机制。动物实验显示,小鼠持续口服 LZ-8一周後,Treg细胞在全身循环系统中的比例明显升高;与此同时,肠道淋巴结中的「耐受性树突细胞(CD103⁺ DCs)」数量亦明显上升,其成熟速度也明显加快(可更快发挥诱导T细胞分化的功能),而其他具有抗感染功能的树突细胞亚群则不受影响。
体外实验则发现,LZ-8可透过Dectin-1受体直接活化耐受性树突细胞,被LZ-8活化的耐受性树突细胞亦可促使Treg细胞显着增殖。由於Treg细胞能抑制Th1与 Th17细胞介导的发炎反应,因此可以推测,吃进肚里的LZ-8是透过活化这类耐受性树突细胞,间接调节T细胞亚群,使小鼠皮肤对乾癣诱发因子(IMQ)表现出更高的耐受力,减轻症状发作时的严重程度(图2)。
先前已有研究团队使用同一来源的LZ-8证明,这个活性蛋白可以透过保护肠道黏膜屏障的完整性,减轻化疗药CPT-11损伤肠道的副作用;如今的研究则是证明LZ-8可以透过肠道免疫的调节作用,让皮肤异常发炎造成的乾癣症状不再那麽容易闻风起舞,为乾癣和其他自体免疫疾病提供了值得参考的防治策略。
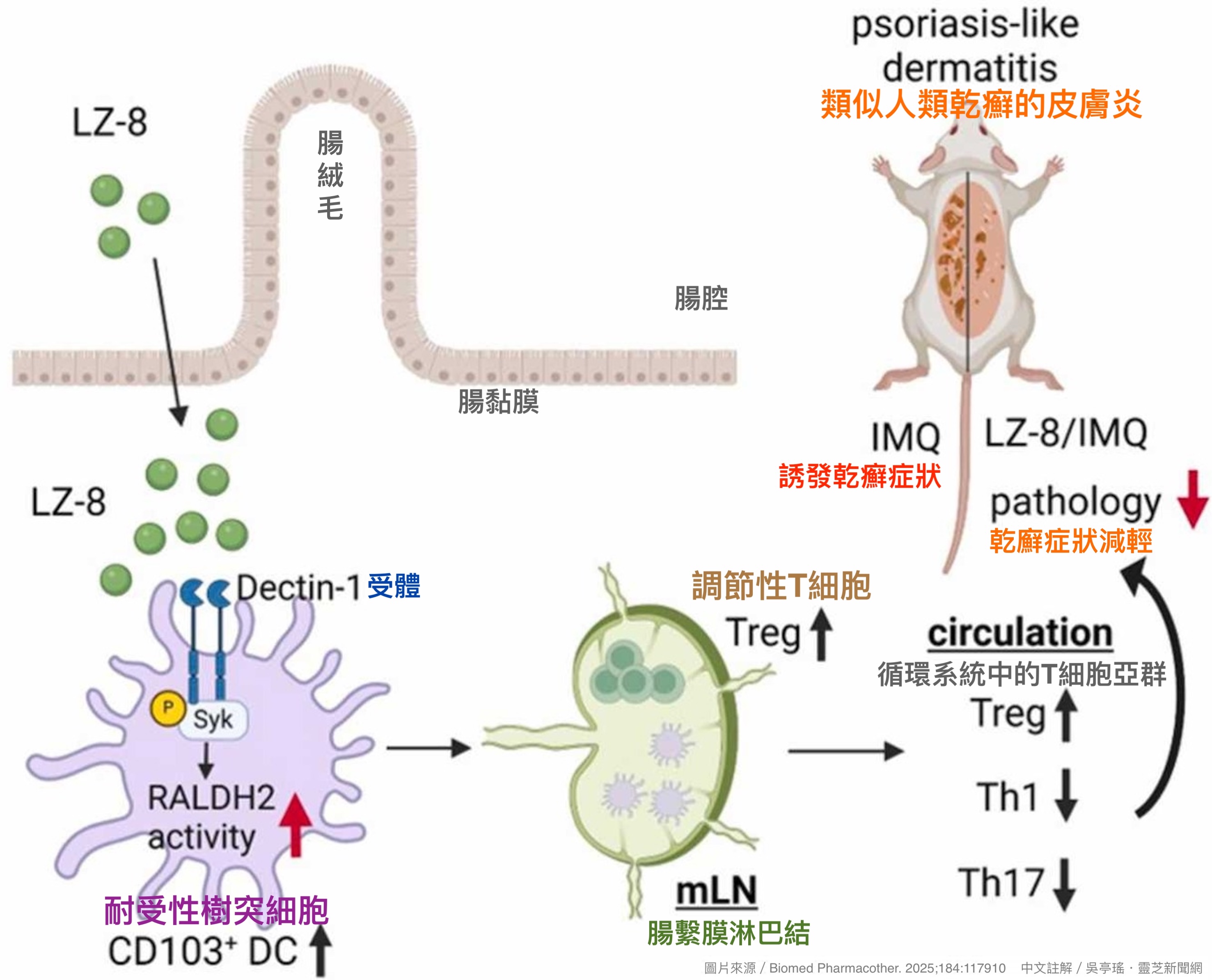
【图2】LZ-8缓和乾癣发作的免疫调节机制示意图:LZ-8诱过Dectin-1受体活化耐受性树突细胞,被活化的耐受性树突细胞迁移至邻近的淋巴结,诱导待命中的 T 细胞分化出更多Treg细胞。Treg细胞的增加会抑制Th1与Th17细胞介导的发炎反应,进而提高皮肤对乾癣诱发因子(IMQ)的耐受力,减轻相关症状的严重程度。
〔资料来源〕Chen-Yu Wang, et al. The fungal protein Lingzhi-8 ameliorates psoriasis-like dermatitis in mice through gut CD103+ tolerogenic dendritic cells, retinaldehyde dehydrogenase 2, and Dectin-1. Biomed Pharmacother. 2025 Mar:184:117910. doi: 10.1016/j.biopha.2025.117910.


