脑部受到撞击的当下不觉得怎麽样,但几天後却开始出现头晕、头痛、记忆变差......甚至连运动协调能力都受到影响,这些情况往往是撞击後没有适当处置或处置方法成效不彰所引发的二次伤害。脑部受创也许很难避免,但二次伤害却有机会避免,虽然并不容易。今年五月由中原大学招名威副教授、曾嘉仪副教授共同发表在《Molecular and Cellular Neuroscience》研究就在告诉我们,口服小孢子灵芝免疫调节蛋白质GMI可以预防或减轻创伤性脑损伤的二次伤害,进而保护神经认知功能相关的记忆能力,而且事前预防和事後治疗并用的保护效果更好。
文/吴亭瑶

不同於阿兹海默症(β类淀粉蛋白沉积)或老化(身体中和自由基的能力衰退)对於脑神经的伤害犹如温水煮青蛙,因跌倒、车祸、运动等外力撞击对脑神经的伤害(以下称为「创伤性脑损伤」,即简称为TBI的traumatic brain injury)则立即的有如热锅上的蚂蚁,而且还可能因为发炎不止、氧化压力升高而酿成二次伤害。
由於成年後脑神经细胞的再生和修复能力都很低,很难长出新的神经细胞取代损伤的神经细胞,更难重建断线的神经通讯网络,因此如何预防或减轻二次伤害,就成了治疗创伤性脑损伤的重中之重。
先前已有许多研究证实,由111个胺基酸组成的小孢子灵芝免疫调节蛋白质GMI小孢子灵芝免疫调节蛋白质GMI(Ganoderma microsporum immunomodulatory protein),不论是抑制癌转移、减轻化疗造成的肠黏膜或口腔黏膜损伤、改善溃疡性大肠炎,抑或防止神经发炎、避免PM2.5危害胎儿脑部,都可看到它的抗氧化或抗发炎作用在其中的卓越贡献。
所以,GM的抗氧化、抗发炎也能从预防或治疗的途径,降低创伤性脑损伤可能造成的伤害吗?
今年(2022)五月,中原大学生物科技学系招名威副教授和生物医学工程学系曾嘉仪副教授共组的团队在《Molecular and Cellular Neuroscience》(分子和细胞神经科学)发表的研究首度证实,「口服GMI」可以预防或减轻创伤性脑损伤的二次伤害,进而保护神经认知功能相关的记忆能力,而且比起创伤发生後才以GMI治疗,创伤发生前就以GMI保养、创伤後再以GMI治疗,对於脑神经的保护效果更好。
脑神经受创→麸胺酸外溢→过多自由基→兴奋性毒性→二次伤害
GMI是如何阻止受创的脑神经遭受「二次伤害」的?GMI又能帮助受损的神经细胞修复到什麽程度?在进一步揭开谜底之前,让我们先了解一下神经细胞的结构特性和二次伤害的主要原由。
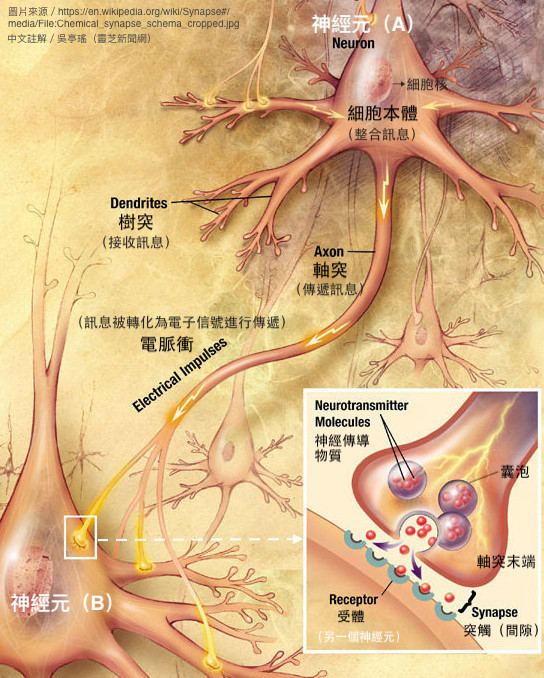
神经细胞的基本构造和讯息传递
(资料来源/Wikimedia Commons)
神经细胞(即神经元)的结构可分为两大部分,其一是拥有细胞核、负责整合讯息和发布指令的「细胞本体」,其二则是从细胞本体往外延伸、负责接收讯息(如树突)或传递讯息(如轴突)的突起,统称「神经突」。如果受创的是细胞本体,基本上就没救了;如果损伤的是神经突,就有机会修复或再生。
神经细胞死亡有可能发生在创伤当下,更可能肇因於麸胺酸(glutamate,也称谷氨酸或谷胺酸)从受损的神经细胞溢出所导致的二次伤害。
麸胺酸是大脑最主要、也是学习记忆不可或缺的兴奋性神经传导物质,它原本被储存在轴突末端的囊泡里,当神经细胞要传递讯息时,才会被释放到神经细胞外(突触间隙)去敲开另一个神经细胞的大门(受体),一旦任务成就会以毫秒的极快速度被回收再利用。
也就是说,正常情况下神经细胞外的麸胺酸会控制在一个水平,当它因为神经细胞受损而大量溢出时,就会使神经细胞「过度兴奋」进而产生过多的自由基(如活性氧),不仅会「毒死」自己,死掉後溢出麸胺酸又会扩大伤害范围。
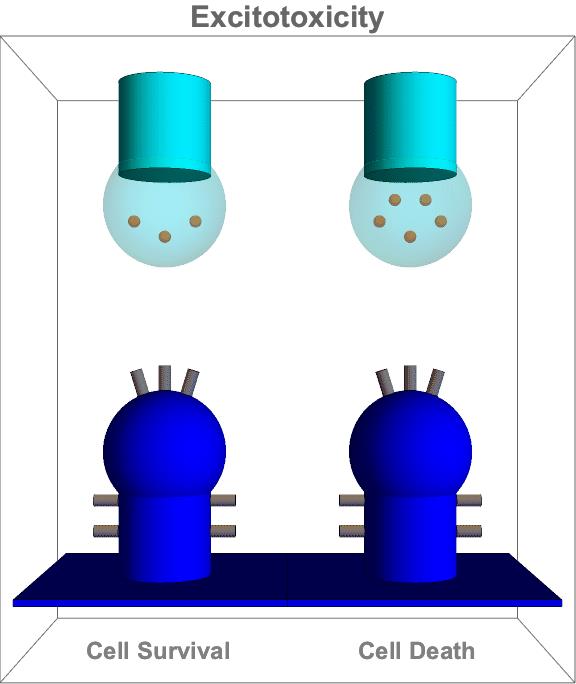
麸胺酸的一体两面:神经讯息传导(细胞存活)vs. 神经兴奋性毒性(细胞死亡)
(图片来源/Wikimedia Commons)
GMI能保护脑神经免於创伤後的二次伤害
本研究的科研团队即在体外模拟这种创伤後由麸胺酸造成「兴奋性毒性(excitotoxicity)」的环境,观察GMI能否对大鼠的脑神经有保护作用。结果发现,如果神经细胞在遭受麸胺酸轰炸(10分钟)之前和之後都能用GMI处理(一起培养24小时),细胞内的活性氧(ROS)自由基会被控制在正常水平,细胞的存活率甚至不减反增。
有趣的是,如果只是把神经细胞和GMI一起培养(48小时),神经细胞可以活得很好(代表GMI对神经细胞没有毒性)但增生的数量却很有限。这似乎在暗示GMI对神经细胞并非一味的刺激细胞增生,而是视情况需要才会有所动作。
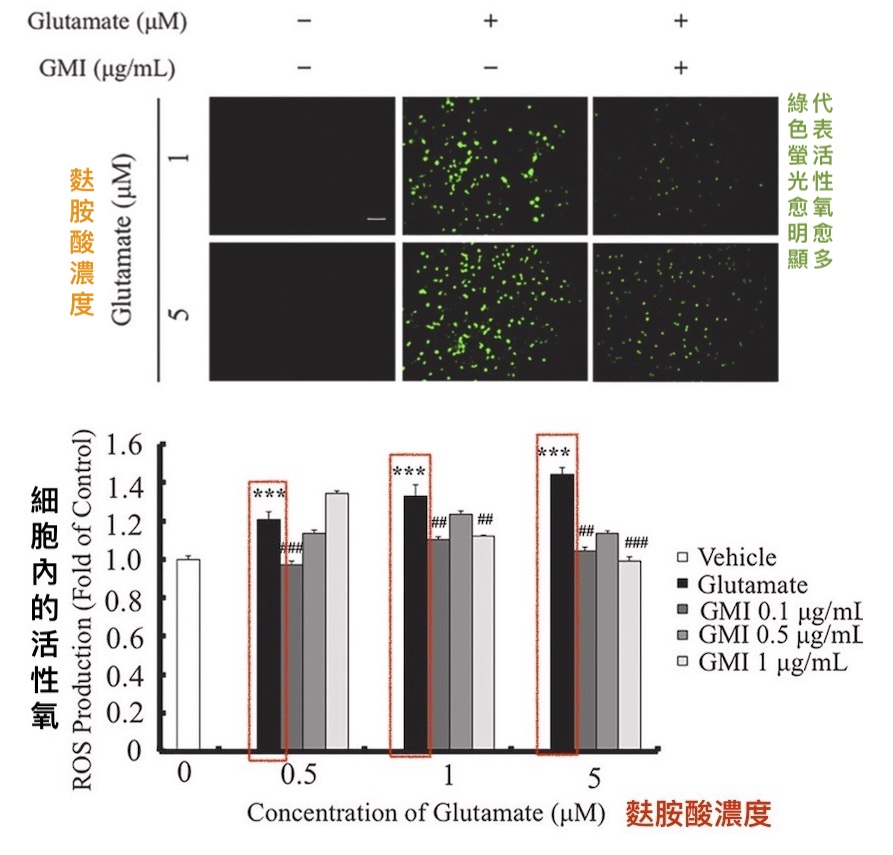
GMI能在麸胺酸造成的兴奋性毒性中
避免大鼠脑神经细胞产生过多的活性氧自由基
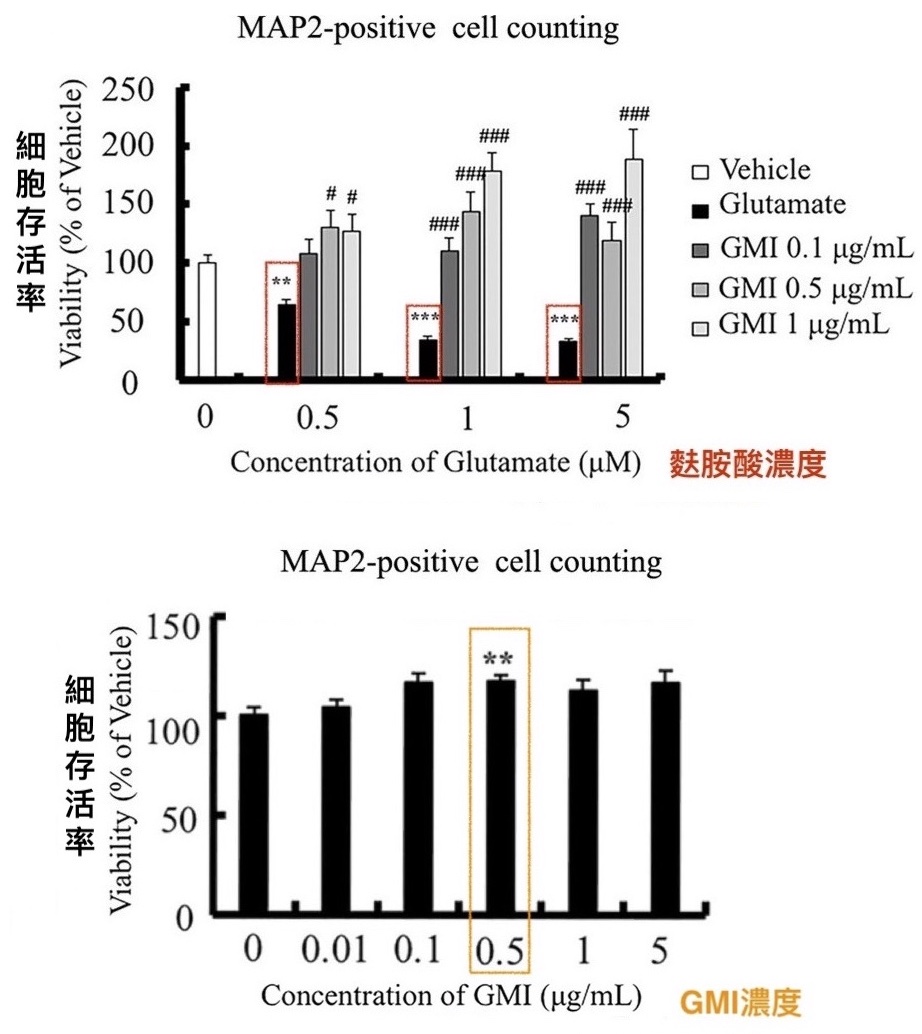
不论有没有麸胺酸造成的兴奋性毒性威胁
GMI都能保障大鼠脑神经细胞的存活率
GMI能促进受损的神经突再生
脑神经受伤表现除了神经细胞死亡之外,还有一种状况是轴突(神经纤维)断裂,毕竟负责传输讯息的它们可是神经细胞最长的结构。死掉的神细胞不可能复活,但断掉的轴突却有修复和再生的可能。
根据本研究在体外模拟神经突受损断裂的实验显示,倘若在受损断裂发生之前和之後都能用GMI处理神经细胞(一起培养24小时),神经突(树突+轴突)的数量虽然没什麽变化,但神经突的整体长度却显着增加,说明GMI有潜力促进受损的轴突再生。

GMI保护大鼠脑神经受损後的再生能力
GMI能减轻创伤性脑损伤对记忆功能的损害
脑部创伤和其他脑部疾病之所以不易治疗,很大一部因素就卡在「血脑屏障」。也就是除了氧、二氧化碳和血糖之外,脑血管几乎不会让任何物质(包含大部分的药物和蛋白质)随身体的血液循环进入大脑,其目的在确保大脑的独立运作,但也加深了治疗脑损伤的困难度。
因此从实际应用的角度思考,GMI在上述体外实验对脑神经的保护,有可能在体内发挥作用吗?毕竟GMI本身就是个蛋白质啊!虽然它的分子结构很小。
这就是GMI有趣的地方。因为根据研究者以成年大鼠挑战水迷宫的记忆能力评估结果显示,不论是脑损伤发生之前一个月和之後一个月都口服GMI预防和治疗并用,还是在脑损伤发生後才口服GMI治疗一个月,GMI都能保护大鼠的记忆功能。只是相比之下,预防和治疗并用的效果明显优於事发後再来治疗。
在预防和治疗并用的组别中,GMI每天只需0.33 μg/Kg的剂量就能让脑损伤的大鼠和没有脑损伤的大鼠保有一样记忆能力,但这样的剂量在治疗组则没有保护效果;如果将预防和治疗并用的GMI剂量提高100倍(每天口服33 μg/Kg),则能让脑损伤大鼠的记忆能力表现得比没有受到脑损伤的大鼠还要好,而这样的剂量在治疗组只能让脑损伤大鼠的表现略优於未治疗者,还比不上没有脑损伤的大鼠。
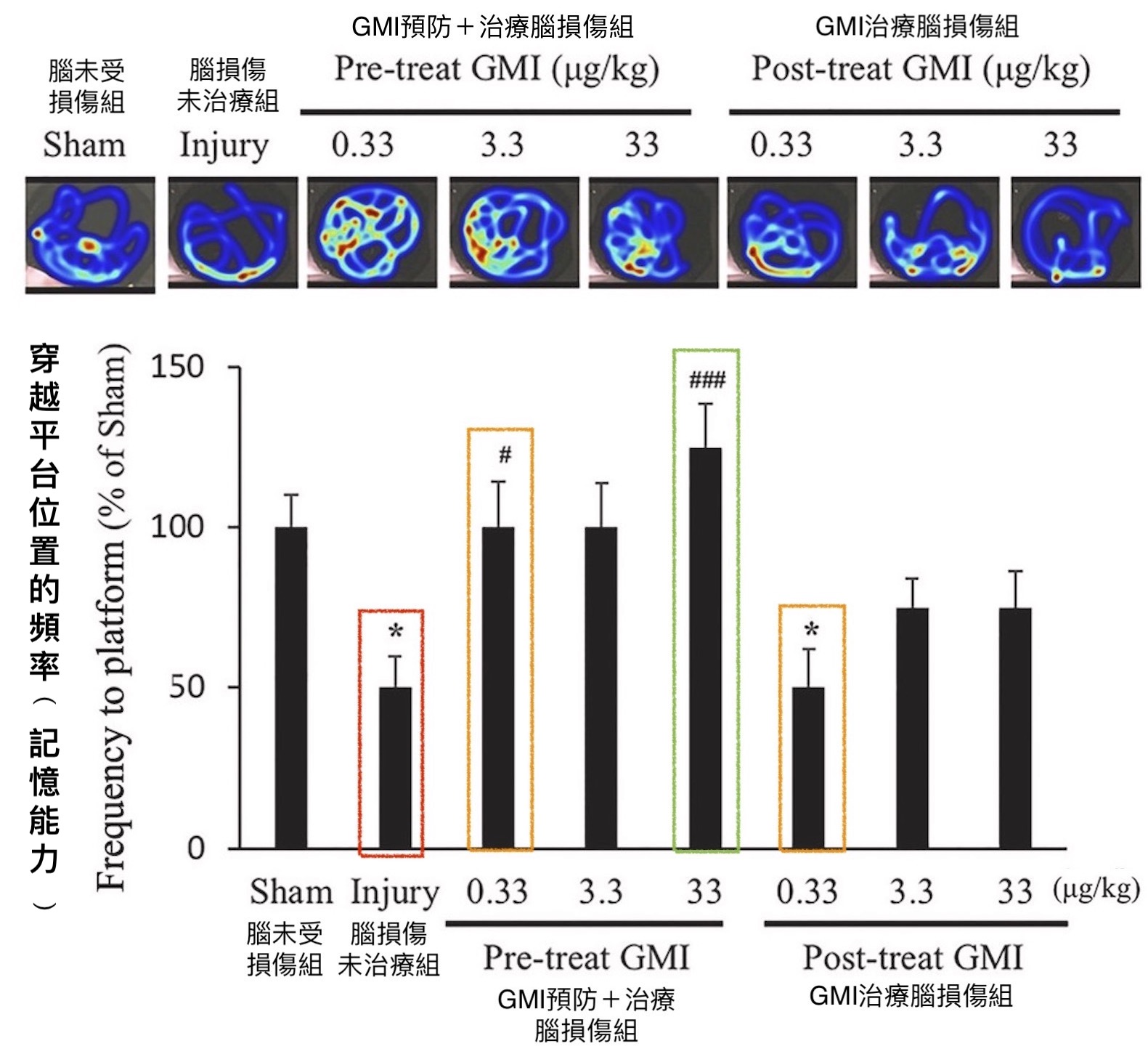
GMI能保护脑损伤大脑的记忆能力(认知功能)
〔说明〕在脑损伤发生第25天开始,连续4天让大鼠在水迷宫中练习寻找固定於水面下的休息平台,每天练习4次,再於第29天将平台移开,记录大鼠60秒内穿越平台原来所在位置的频率,频率高代表大鼠愈确信自己的记忆力,由此即可窥知大脑认知功能(掌管记忆)的受损程度。图上方的影像为大鼠寻找平台的轨迹记录,红色为频繁经过或长时间逗留的热区,图下方则是将影像记录结果数据化,以脑未受损伤的大鼠表现为基准进行比较。
GMI可加速损伤的大脑组织修复
为什麽有GMI能帮助脑损伤大鼠保有比较好的记忆能力(认知功能)?研究者把各组大鼠的脑袋打开来仔细研究,结果发现,这些经过一个月休养生息的损伤大脑,虽然在外观和重量上没有明显差别,但细究损伤部位(大脑皮质和海马回)的组织结构则会发现,有GMI保护的大脑恢复状况比较好,尤其是预防和治疗并用者,又比只用GMI治疗者恢复得更好。
而GMI之所以能加速损伤的大脑组织修复,除了与增加超氧化物歧化酶SOD-1(可中和自由基)进而提高神经细胞的抗氧化能力有关之外,在预防和治疗并用的大鼠身上还可观察到,经常伴随随脑损伤出现且会进一步促进发炎造成脑损伤恶化的星状胶细胞过度增生,以及小胶质细胞过度活化,也会被GMI控制在相对低的水平。
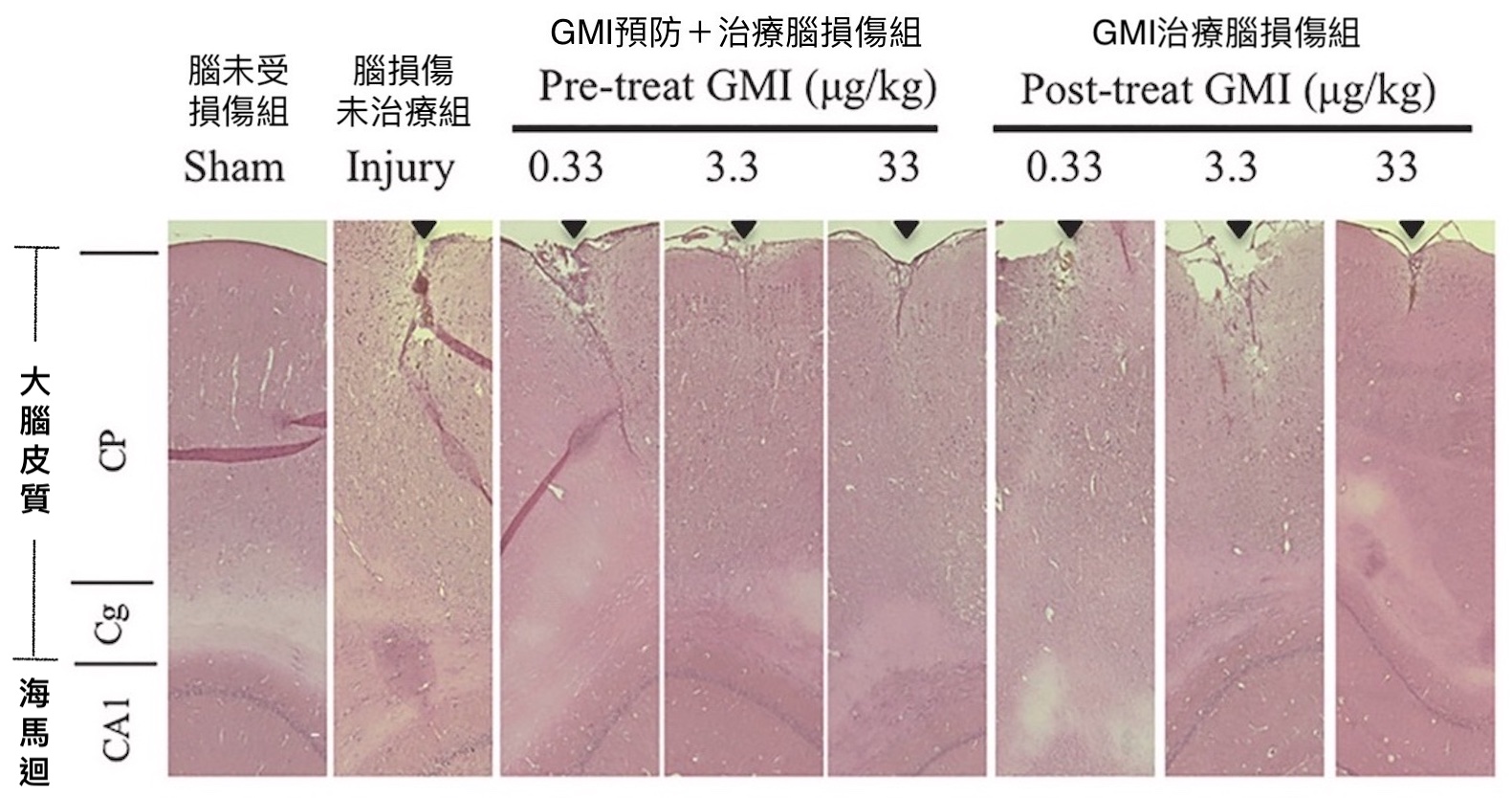
GMI能帮助损伤的大脑皮质和海马回加速修复
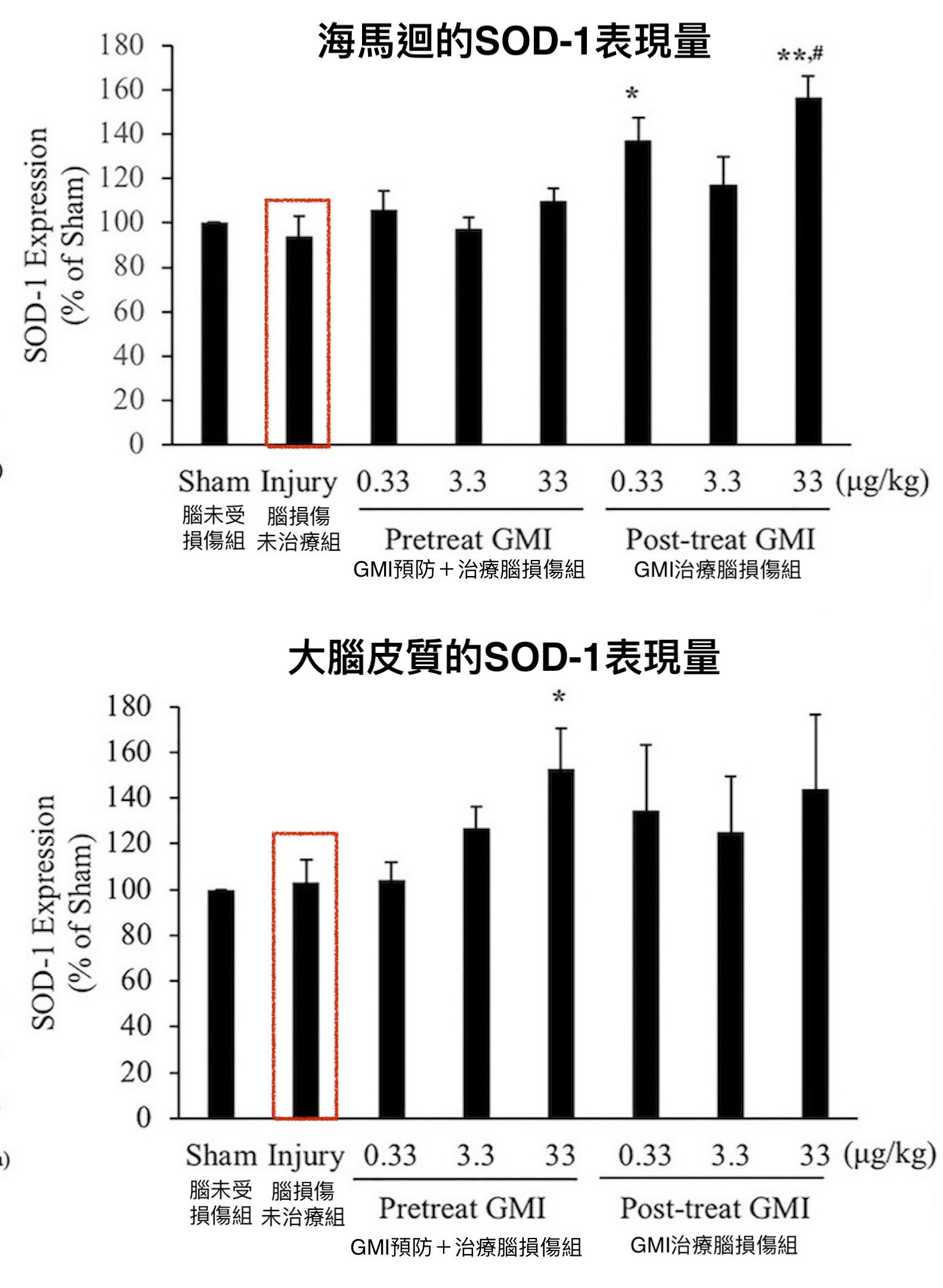
GMI能增加大脑皮质和海马回的抗氧化酵素SOD-1
〔说明〕大脑皮质:包裹在大脑最外面的皱褶状结构,执掌储存记忆,也称灰质或皮层;海马回:位於大脑皮质下方,负责形成记忆。上图和下图分别展现的是脑损伤发生一个月後大鼠大脑的组织冷冻切片H&E染色影像和抗氧化酵素SOD-1表现量。
GMI是如何跨越血脑屏障的?
从细胞实验显示的GMI能促进神经再生和避免麸胺酸的兴奋性毒性对神经细胞造成二次伤害,到动物实验显示的口服GMI能加速脑伤修复、保护记忆(认知)功能,GMI显然为创伤性脑损伤提供了另类的防治思维。
整体而言,创伤发生後才口服GMI治疗的效果相对有限,事前和事发後都持续口服GMI所产生的保护作用则是令人眼睛为之一亮,而且似乎不需追求高剂量,只要低剂量或中剂量(每天0.33 μg/Kg或3.3 μg/Kg)就有不错效果。但不管是哪种剂量,其实就动物实验来说都很低,因为这里使用的剂量单位可不是大家常见的毫克(mg),而是仅有其千分之一的微克(μg)。
只是进到胃肠道的GMI到底是如何跨越血脑屏障,让创伤性脑损伤的警报得以解除,实在令人玩味。会不会GMI也像那些神经传导物质,只是负责敲开某个或某些讯息之门,并没有实际参与游戏,还是两者兼而有之?期待未来能有更明确的解答。

小孢子灵芝免疫调节蛋白质GMI的立体构形与胺酸酸序列
〔资料来源〕Ming-Wei Chao, et al. Immunomodulatory protein from Ganoderma microsporum protects against oxidative damages and cognitive impairments after traumatic brain injury. Mol Cell Neurosci. 2022 May; 120:103735. doi: 10.1016/j.mcn.2022.103735.


